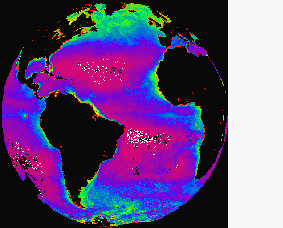
Distribución global de la clorofila en la Tierra. Aparece en color verde brillante, y es notable su concentración en las zonas templadas y polares de los océanos. En las zonas costeras la clorofila es también abundante, pero parte del efecto en la fotografía es debido a que los sedimentos tienen una absorción semejante. Fotografía de Commitee on Earth Observation satellites



 Volver a: Bioquímica de los alimentos
Volver a: Bioquímica de los alimentos